
NO3 hóa trị mấy? Nguồn gốc phát sinh NO3
NO3 là hóa chất gặp nhiều trong các dạng bài tập hóa học. Vậy NO3 là gì? NO3 hóa trị mấy và nguồn gốc phát sinh NO3 như thế nào? Các bạn hãy cùng theo dõi nội dung được VietChem chia sẻ dưới đây để hiểu rõ hơn về NO3.
1. NO3 là gì?
Trước khi tìm hiểu NO3 hóa trịmấy hãy cùng phân tích chi tiết NO3. Theo đó, NO3 là chất hóa học gồm một nguyên tử nitơ và 3 nguyên tử oxi bao quanh trên cùng mặt phẳng tam giác. Đây là bazơ liên hợp của axit nitric, còn có nhiều tên gọi khác nhau như: Nitrate, nitrat với khối lượng phân tử là 62.
Trong nước, dưới tác động của các vi khuẩn từ NH3 phân hủy tạo thành NO2. NO3 là sản phẩm cuối cùng của phản ứng oxi hóa này.
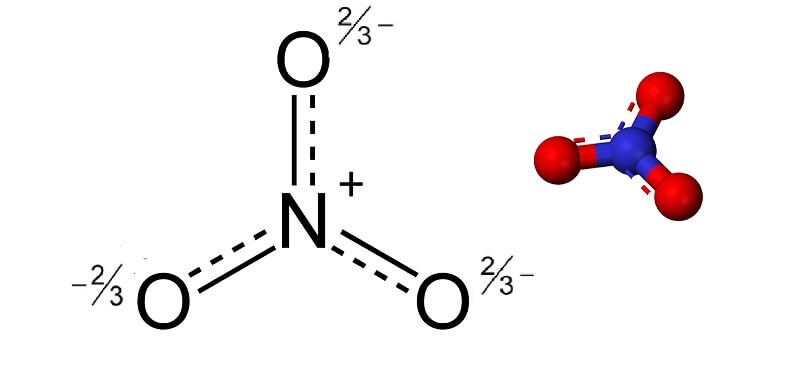
NO3 là chất hóa học gồm 1 nguyên tử Nitơ và 3 nguyên tử oxy
2. NO3 hóa trị mấy
NO3 chính là ion nitrat với cấu tạo gồm 1 nguyên tử Nitơ (N) và 3 nguyên tử Oxi (O). Trong đó, ion nitrat có nitơ mang hóa trị -3 và oxi mang hóa trị -2. Tuy nhiên, có tới 3 nguyên tử oxi cùng với hóa trị (-2), nitơ chỉ có 1 nguyên tử với hóa trị -3.
Vậy ion nitrat có tổng hóa trị là 3 x (-2) + (-3) = (-9). Trong ion nitrat, để tạo ra điện tử âm (-1) thì phải giảm điện tử từ hóa trị (-9) xuống (-1). Vì thế hóa trị của NO3 là -1.
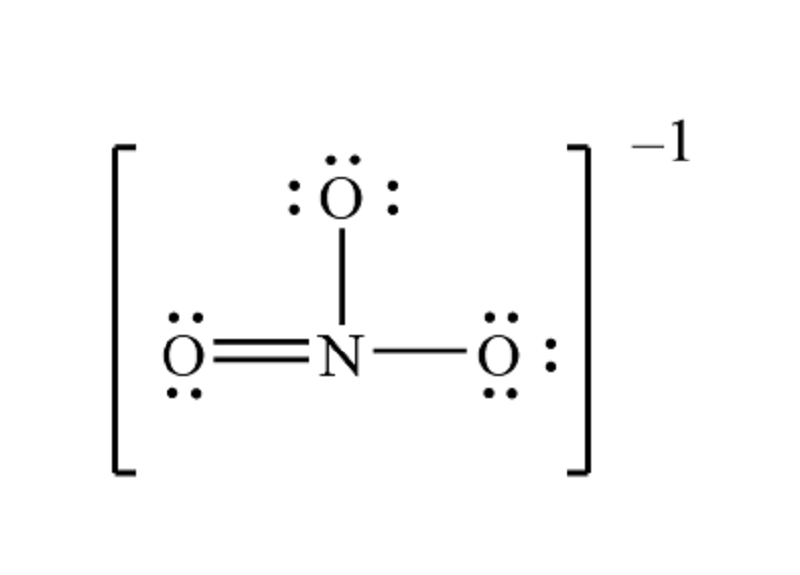
NO3 có hóa trị -1
3. Nguồn gốc phát sinh NO3
NO3 hóa trị mấy đã được phân tích chi tiết ở phần trên. Vậy nguồn gốc phát sinh NO3 từ đâu thì các bạn hãy cùng khám phá dưới đây:
- NO3 là nitrat có thể được tạo thành từ nitơ tự nhiên trong lòng đất. Đây là chất khí chiếm tỉ lệ cao trong khí quyển nên quá trình phát sinh nitrate xảy ra thường xuyên.
- Trong đồ uống hay thực phẩm hàng ngày của con người cũng có chứa một hàm lượng NO3 nhất định. Tuy nhiên, chúng không gây hại cho sức khỏe nếu hấp thụ ít trong cơ thể.
- Ngoài tự nhiên, cây cối cũng thường xuyên hấp thu NO3 trong đất. Khi đó, trong lá hay quả của cây sẽ có một dư lượng không đáng kể chất này.
- Quá trình hình thành NO3 có thể diễn ra khi phân hủy xác động thực vật. Hay tạo ra trong quá trình vi sinh vật chuyển hóa phân bón.
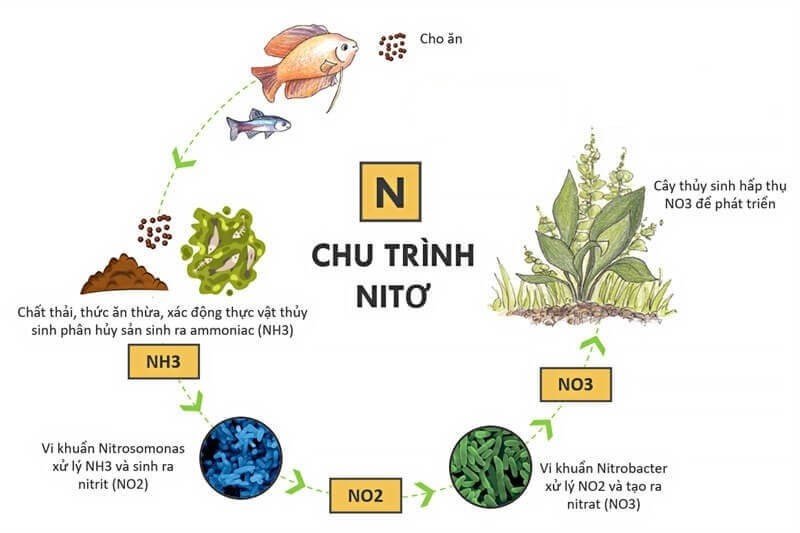
Chu trình sản sinh NO3 trong đất
4. Tính chất hóa học của NO3
Tan trong dung dịch kiềm
NO3 - có thể oxi hóa được các kim loại lưỡng tính hay tan trong dung dịch kiềm. Phương trình phản ứng: 8Al + 3NO3- + 5OH- + 2H2O → 8AlO2- + 3NH3.
Trong đó, NH3 tạo thành là chất khí bay hơi.
Tham gia phản ứng nhiệt phân
- Nhiệt phân muối nitrat hoạt động trước Mg dưới điều kiện nhiệt độ cao. Phương trình phản ứng:
Nitrat → Nitrit + O2
Ví dụ: 2KNO3 → 2KNO2 + O2
- Đối với trường hợp muối nitrat hoạt động sau Cu (Đồng) kết thúc phản ứng tạo thành kim loại:
Nitrat -> Kim loại + NO2 + O2
Ví dụ: AgNO3 → 2Ag + 2NO2 + O2
- Đối với trường hợp muối nitrat của kim loại trong khoảng từ Mg đến Cu, kết quả thu được là oxit kim loại và NO2, O2. Phương trình phản ứng:
Nitrat → Oxit kim loại + NO2 + O2
Ví dụ: 2Cu(NO3)2 → 2CuO + 4NO2 + O2
Phản ứng với axit
Phương trình phản ứng:
3Fe2+ + NO3- + 4H+ → 3Fe3+ + NO↑ + 2H2O
3Cu + 2NO3- + 8H+ → 3Cu2+ + 2NO↑ + 4H2O
5. Cách nhận biết ion nitrat
Nhận biết ion nitrat trong môi trường axit sử dụng vụn đồng và axit sunfuric loãng, đun nóng. Quá trình phản ứng thấy xuất hiện dung dịch màu nâu. Trong không khí thấy có chất khí không màu bay lên hóa nâu đỏ ngay sau đó.
Phương trình phản ứng:
- Phương trình 1: 3Cu + 8H+ + 2NO3- → 3Cu2+ (dd màu xanh) + 2NO↑ + 4H2O
- Phương trình 2: 2NO + O2 (không khí) → 2NO2 (màu nâu đỏ)
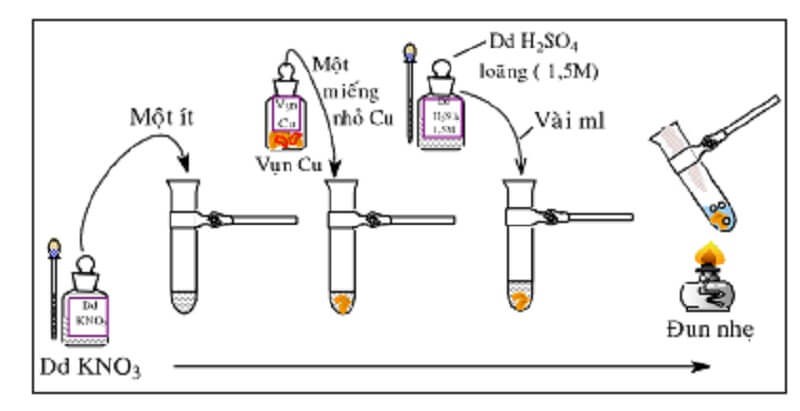
Phương trình phản ứng nhận biết NO3
6. Tác hại của NO3
Biết được tác hại của NO3 sau khi tìm hiểu NO3 hóa trị mấy sẽ giảm thiểu tối đa nguy hiểm tới sức khỏe, sinh vật và môi trường sống. Cụ thể:
6.1. Tác hại của NO3 với con người
Đối với các loại thực phẩm có hàm lượng nitrate cao hơn ngưỡng 10 mg/l không nên cho trẻ sử dụng. Kể cả nước uống vì nó sẽ gây nên tình trạng da xanh ở trẻ.
Cơ thể hấp thụ dư thừa NO3 có thể làm suy giảm chức năng vận chuyển oxy. Điều này dẫn đến lượng oxy lên não không đủ. Tình trạng kéo dài sẽ nguy hiểm trực tiếp đến tính mạng, thậm chí tử vong.
6.2. Tác hại của NO3 với sinh vật
Nồng độ NO3 cao trong quá trình nuôi trồng thủy sản sẽ làm giảm sự sinh sản, phát triển. Từ đó, ảnh hưởng trực tiếp đến cây trồng, vật nuôi. Điển hình như: Tôm bị cụt râu, cá bỏ ăn, bơi chậm chạp, nhợt nhạt và chết.

Lượng NO3 dư thừa gây hại cho sinh vật
6.3. Tác hại của NO3 với môi trường
Nồng độ NO3 quá nhiều trong không khí khiến cho cây cối không hấp thu hết được nitrate. Chúng sẽ ngấm vào lòng đất gây nguy cơ ô nhiễm nguồn nước.
Từ những phân tích chi tiết trong bài viết trên đã giúp các bạn hiểu được NO3 hóa trị mấy. Đây là chất hóa học gây hại cho sức khỏe con người và môi trường nên cần sử dụng đúng liều lượng. Nếu muốn tìm hiểu nhiều hơn về NO3, các bạn hãy gọi điện thoại đến VietChem theo số hotline để được nhân viên hỗ trợ.
Link nội dung: https://brightschool.edu.vn/no3-hoa-tri-may-nguon-goc-phat-sinh-no3-a22413.html